属于国家管控危险化学品,根据相关法规和网安部门规定,本网站不提供该产品相关销售信息。
近日,贝达药业发布最新年报,2023年全年,其总营收24.56亿元,同比增长3.35%;净利润3.48亿元,增长139.33%;归母扣非净利润为2.63亿元,大幅增长768.85%。经历了去年可怕的净利润下滑之后,贝达药业通过调整策略药业,也得益于多款已上市产品的给力销售,终于走出至暗时刻,重新步入增长正轨。
近日,贝达药业发布最新年报,2023年全年,其总营收24.56亿元,同比增长3.35%;净利润3.48亿元,增长139.33%;归母扣非净利润为2.63亿元,大幅增长768.85%。经历了去年可怕的净利润下滑之后,贝达药业通过调整策略,也得益于多款已上市产品的给力销售,终于走出至暗时刻,重新步入增长正轨。
曾经的贝达药业,仅靠一款埃克替尼就可以包打天下。但这样“躺赚”的日子在进入创新药时代后已一去不复返,迎接贝达药业的是一段青黄不接的尴尬期。
好在这样的尴尬并没有持续太久,截至目前,贝达药业已有另外4款产品获批上市接力埃克替尼。
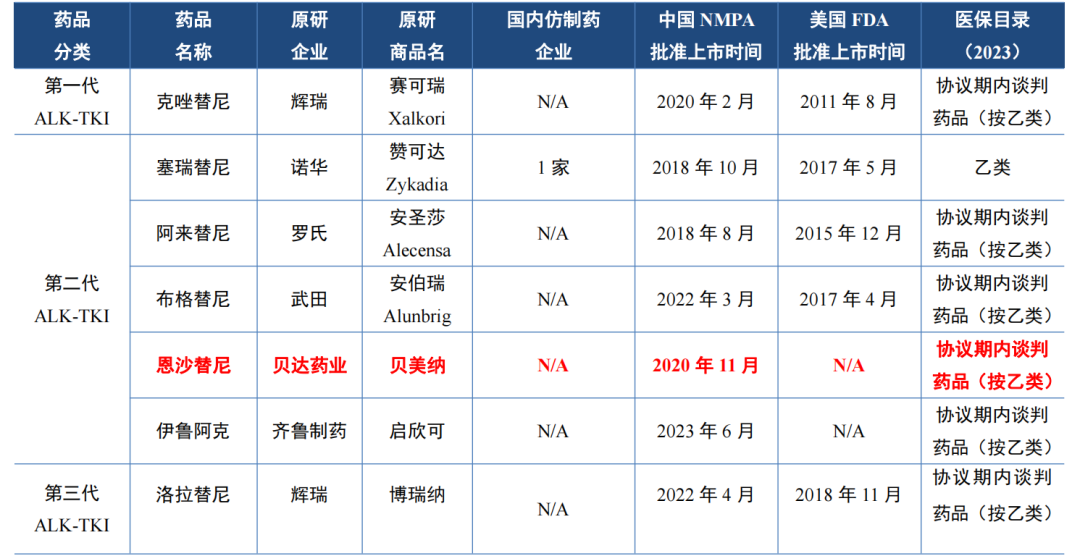
恩沙替尼是第一个用于治疗ALK阳性晚期非小细胞肺癌(NSCLC)的国产1类新药,于2020年11月获批。目前获批的适应症包括适用于此前接受过克唑替尼治疗后进展的或者对克唑替尼不耐受的ALK阳性的局部晚期或转移性NSCLC患者的治疗、适用于ALK阳性的局部晚期或转移性NSCLC患者的治疗;用于ALK阳性的NSCLC术后辅助治疗适应症)已完成II-IIIB期受试者入组。
一是因为中国非小细胞肺癌ALK突变患者总量不多,二是因为竞争者日众。目前,在我国上市的ALK抑制剂已达到7款,此外中国正在进行临床试验的ALK抑制剂还有10余款,恩沙替尼的处境不容乐观。
甲磺酸贝福替尼(赛美纳)是贝达药业拥有的全新的、自主知识产权的国家1.1类创新药,是一种新型的国产第三代强效、高选择性的小分子口服EGFR-TKI,能够同时结合EGFR敏感突变和T790M突变。于2018年12月从益方生物License-in,贝达药业拥有大中华区的独家权利。
2023年5月,贝福替尼顺利获批,适应症为用于既往经EGFR-TKI治疗出现疾病进展,并且伴随EGFR T790M突变阳性的局部晚期或转移性NSCLC患者的治疗;2023年10月用于具有表皮生长因子受体外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性NSCLC成人患者的一线治疗适应症也得到获批。
目前,用于EGFR敏感突变阳性的IB-IIIB(T3N2M0)期伴有EGFR基因敏感突变NSCLC术后辅助治疗和MCLA-129、甲磺酸贝福替尼胶囊联合用药的临床试验正在进行。
在此前一线和二线治疗临床研究中,贝福替尼均创下相同治疗情景下PFS(无进展生存期)的新纪录,已被写入《IV期原发性肺癌中国治疗指南(2023版)》等权威指南中。
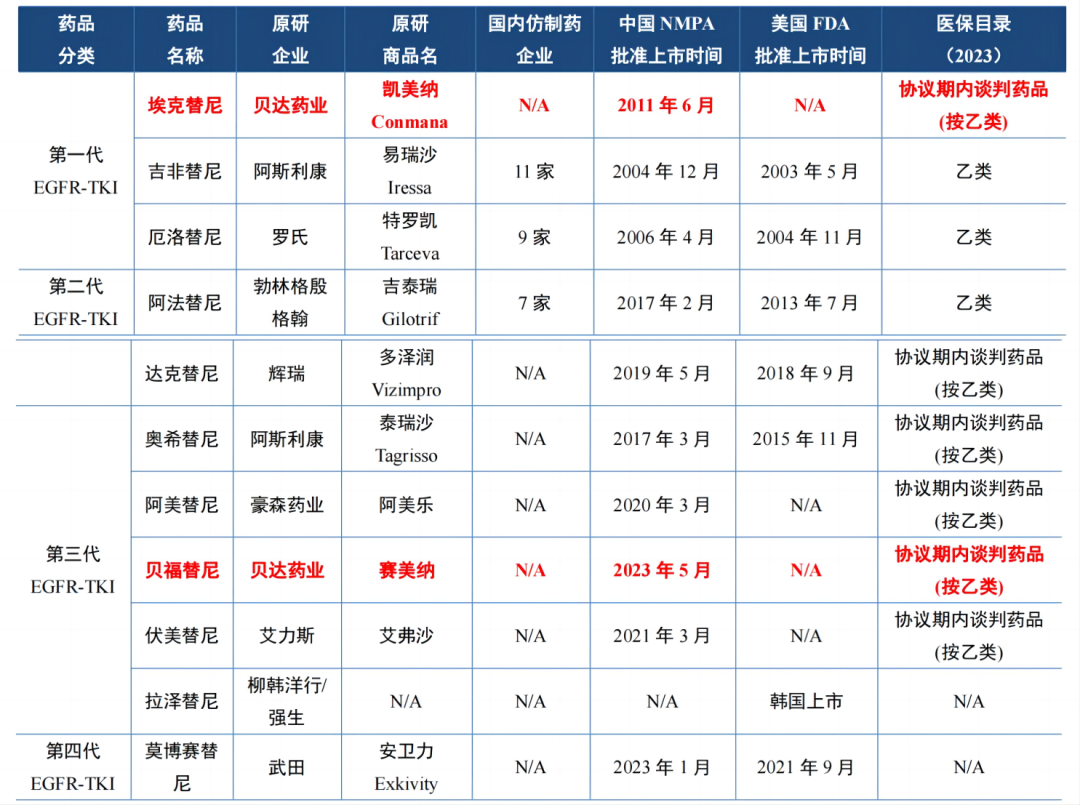
尽管贝福替尼十分优秀,但奈何市场格局已然十分拥挤。目前国内外已上市的非小细胞肺癌EGFR-TKI已超过10种,其中一代3个,二代2个,三代5个,四代1个。
虽然贝达药业的埃克替尼仍然占有我国EGFR-TKI市场较大的比重,但当前的格局中,第三代EGFR-TKI占主导地位,其中奥希替尼的强势地位很难撼动。同样作为第三代EGFR-TKI,贝福替尼的国产竞争对手还包括翰森制药的阿美替尼和艾力斯的伏美替尼。阿美替尼背靠翰森制药强大的销售网络,虽然未公布2023年销售额,但从往年成绩来看,销售额在20亿元以上;伏美替尼2023年的成绩更是直接“爆炸”,达到了19.72亿元,增长1.48倍。
面对如此强劲的对手,贝福替尼“压力山大”。不过贝福替尼的优势在于,借助埃克替尼的销售渠道加成,或许将后来居上也未可知。
当然,恩沙替尼和贝福替尼面临的竞争,虽然较当年埃克替尼大得多,但不可否认的是这两款产品都十分优秀,只是时代的因素增加了些许不确定性而已。尽管存在这样的不确定性,但短期内,这两款产品将共同支撑起埃克替尼被替代掉的营收,成为贝达药业的支柱。
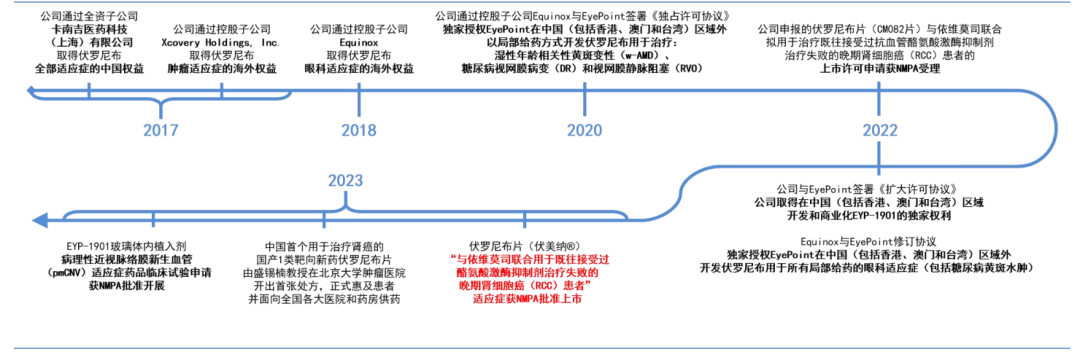
伏罗尼布(伏美纳)是具有全新化学结构的新一代多靶点VEGFR/PDGFR抑制剂,可抑制肿瘤血管生成及生长,用于多种癌症的治疗。针对VEGFR、PDGFR、c-Kit、Flt-3、CSF1R等多靶点,伏罗尼布具有抗血管生成的显著疗效,并且能够满足靶点的特殊PK/PD要求,达到保留活性,降低毒性的目的。
此前,伏美纳联合依维莫司治疗肾癌患者疗效和安全性的II/III期研究CONCEPT在《欧洲癌症杂志》发表。研究数据显示,IRC评估的伏美纳联合依维莫司组中位PFS为10.0个月,显著优于依维莫司单药组的6.4个月;联合组、依维莫司单药组的中位OS分别为30.4个月、25.4个月;伏美纳联合依维莫司的ORR达到24.8%,显著高于依维莫司单药组的8.3%,DCR达到84.2%,也显著高于单药组。
最终于2023年6月,伏罗尼布获批上市,适应症为与依维莫司联合用于既往接受过酪氨酸激酶抑制剂治疗失败的晚期肾细胞癌(RCC)患者。
湿性年龄相关性黄斑变性是一种与老年相关的严重眼科疾病,该疾病主要影响60岁以上的老年人,因此相关药物受到人口老龄化背景的需求驱动。2023年7月,贝达药业与EyePoint共同申报的EYP-1901玻璃体内植入剂病理性近视脉络膜新生血管(pmCNV)适应症药物临床试验申请已获批准开展。
EYP-1901玻璃体内植入剂通过EyePoint专有的可生物降解的缓释技术Durasert E将伏罗尼布注射进入玻璃体内,使伏罗尼布以可控且可耐受的方式持续地在眼部释放。2023年12月,EYP-1901治疗wAMD的II期临床试验DAVIO 2达到所有主要终点和次要终点:主要终点BCVA的变化对比阿柏西普对照组,EYP-1901剂量组(2mg和3mg)分别相差-0.3和-0.4个字母,达到了统计学上的非劣效结论;治疗负担(注射频率)分别减少了89%和85%;65%和64%的受试者可以六个月内无需进行抗VEGF补救治疗。
作为中国首 个用于治疗肾细胞癌的国产1类靶向新药,以及有望拓展至眼科领域相关适应症,伏罗尼布很有想象力空间。
除了上述三款已上市产品,在贝达药业近几年用力“砸钱”之下,诸多管线年,贝达药业研发投入占营业收入的比例高达38.32%、41.12%及40.80%;2023年全年研发投入达10亿元,增长2.53%。根据官网数据,贝达药业共有16个处于临床各阶段的项目。
BPI-16350是贝达药业自主研发的全新的、拥有完全自主知识产权的CDK4/6抑制剂,拟单药或与激素疗法联合,主要用于治疗HR阳性/HER2阴性的晚期或转移乳腺癌患者,还可能用于Rb+的其他癌症的一、二线或联合治疗。
BPI-361175是第四代EGFR-TKI,拟治疗携带EGFR C797S突变及其他EGFR相关突变的晚期非小细胞肺癌等实体瘤,已分别于2021年2月和11月获国家药监局和美国FDA批准开展临床试验,正处于临床I期。
就在一周以前,贝达药业开了一场销售团队誓师会,贝达药业董事长助理、丁列明之子丁师哲作了题为《贝达药业未来展望》的主题报告。这份展望很大程度上能反应贝达药业未来的战略规划,报告中提到,未来贝达药业要动态平衡开源节流,引进可持续发展项目,维持并提升目前营收及市场份额,以大博大探索新领域,塑造有力生态环境。结合近段时间以来的一些大动作,我们似乎看到了贝达药业的某种决心。但这份决心是什么,目前还不得而知。后续发展如何,药渡还将持续关注。
更多
创新药太难,门槛过高,仿制药太卷,且难以设立门槛,导致过度...[详细]
2023年,一共49种新药在美国、欧盟和日本首次获批。其中,40个药...[详细]
肠道菌群可以产生多种酶,主要是α-鼠李糖苷酶、β-葡萄糖苷酶、...[详细]
p53再激活剂PC14586(Rezatapopt),打破p53基因突变“不可...
当TP53基因失活后,要使其恢复到正常状态变得极为困难,且没有...[详细]

访问手机版

关注华体会体育最新登录